Вредоносное ПО (malware) - это назойливые или опасные программы,...


КАРБОНОВЫЕ КИСЛОТЫ
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Число карбоксильных групп характеризует основность кислоты.
В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты.
В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
Одноосновные карбоновые кислоты
1.1 Гомологический ряд и номенклатура
Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты

Формула гомологического ряда
Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д.
Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д.
Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:

При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН.
1.2 Физические свойства карбоновых кислот
Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:

Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:

Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:

Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.

На
физических свойствах карбоновых кислот
сказывается значительная степень
ассоциации вследствие образования
водородных связей. Кислоты образуют
прочные водородные связи, так как
связи О-Н в них сильно поляризованы.
Кроме того, карбоновые кислоты способны
образовывать водородные связи с участием
атома кислорода карбонильного
диполя, обладающего значительной
электроотрицательностью. Действительно,
в твердом и жидком состоянии карбоновые
кислоты существуют в основном в виде
циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
Химические свойства
Для кислот характерны три типа реакций: замещения иона водорода карбоксильной группы (образование солей); с участием гидроксильной группы (образование сложных эфиров, галогенангидридов, ангидридов кислот); замещения водорода в радикале.
Образование солей. Карбоновые кислоты легко образуют соли при взаимодействии с взаимодействии с металлами, их оксидами, со щелочами или основаниями, при действии аммиака или аминов:
Соли карбоновых кислот находят широкое применение в народном хозяйстве. Они используются в качестве катализаторов, стабилизаторов полимерных материалов, при изготовлении красок и т.д.
Образование сложных эфиров. Со спиртами кислоты дают сложные эфиры:

Образование галогенангидридов. При действии на кислоты галогенидов фосфора или SОС1 2 получаются галогенангидриды кислот:

Галогенангидриды – очень реакционноспособные вещества, которые применяются для разнообразных синтезов.
Образование ангидридов кислот. Если от двух молекул карбоновых кислот отнять одну молекулу воды (в присутствии водоотнимающих веществ Р 2 О 5 и др.), образуется ангидрид карбоновой кислоты:

Ангидриды кислот, подобно галогенангидридам, очень реакци-онноснособны; они разлагаются различными соединениями с активным водородом, образуя производные кислоты и свободную кислоту:

Галогенирование карбоновых кислот. Водородные атомы углеводородных радикалов в кислотах по реакционной способности подобны атомам водорода в алканах. Исключение составляют атомы водорода, расположенные у α-углеродного атома (непосредственно связанного с карбоксилом). Так, при действии хлора и брома в присутствии переносчиков галогенов (РС1 3 , 1 2 и др.) на карбоновые кислоты или на их хлорангидриды происходит замещение именно α -водородных атомов:

Действие окислителей. Одноосновные карбоновые кислоты, как правило, устойчивы к действию окислителей. Легко окисляются лишь муравьиная кислота (до СО 2 и Н 2 О) и кислоты с третичным атомом углерода в α -положении. При окислении последних получаются α -оксикислоты:

В животных организмах одноосновные карбоновые кислоты также способны окисляться, причем атом кислорода направляется всегда в β-положение. Так, например, в организме больных диабетом масляная кислота переходит в β -оксимасляную кислоту:
Образование кетонов Сухая перегонка кальциевых и бариевых солей карбоновых кислот (кроме муравьиной кислоты) приводит к образованию кетонов. Так, при перегонке ацетата кальция, полученного из СаСО 3 и СН 3 СООН, образуется диметилкетон, при перегонке пропионовокислого кальция - диэтилкетон:

Образование амидов. При нагревании аммониевых солей кислот получаются амиды:
Образование углеводородов. При сплавлении солей щелочных металлов карбоновых кислот со щелочами (пиролиз) происходит расщепление углеродной цепи и декарбоксилирование, в результате чего из углеводородного радикала кислоты образуется соответствующий углеводород, например:
Важнейшие представители
Муравьиная кислота - бесцветная жидкость с резким запахом. Является сильным восстановителем и окисляется до угольной кислоты. В природе свободная муравьиная кислота встречается в выделениях муравьев, в соке крапивы, в поте животных. Применяют муравьиную кислоту при крашении тканей в качестве восстановителя, при дублении кож, в медицине, в различных органических синтезах.
Уксусная кислота - бесцветная жидкость с резким запахом. Водный раствор (70 - 80 %) уксусной кислоты называется уксусной эссенцией, а 3 -5%-ный водный раствор - столовым уксусом.
Уксусная кислота широко встречается в природе. Она содержится в моче, поте, желчи и коже животных, растениях. Образуется при уксуснокислом брожении жидкостей, содержащих спирт (вино, пиво и др.).
Широко используется в химической промышленности для производства ацетатного шелка, красителей, сложных эфиров, ацетона, уксусного ангидрида, солей и т.д. В пищевой промышленности уксусная кислота используется для консервирования продуктов, некоторые сложные эфиры уксусной кислоты применяются в кондитерском производстве.
Масляная кислота представляет собой жидкость с неприятным запахом. Содержится в виде сложного эфира в коровьем масле. В свободном состоянии находится в прогоркшем масле.
2. Двухосновные карбоновые кислоты
Общая
формула гомологического ряда предельных
двухосновных кислот ![]()
Примерами могут служить:

Предельные двухосновные кислоты - твердые кристаллические вещества. Подобно тому, как это отмечалось для одноосновных кислот, предельные двухосновные кислоты с четным числом атомов углерода плавятся при более высокой температуре, чем соседние гомологи с нечетным числом атомов углерода. Растворимость в воде кислот с нечетным числом атомов углерода значительно выше растворимости кислот с четным числом атомов углерода, причем с возрастанием длины цепи растворимость кислот в воде уменьшается.
Двухосновные кислоты диссоциируют последовательно:
Они сильнее соответствующих одноосновных кислот. Степень диссоциации двухосновных кислот понижается с увеличением их молекулярной массы.
В молекуле двухосновных кислот содержатся две карбоксильные группы, поэтому они дают два ряда производных, например средние и кислые соли, средние и кислые сложные эфиры:

При нагревании щавелевой и малоновой кислот легко отщепляется СО 2:
Двухосновные кислоты с четырьмя и пятью атомами углерода в молекуле, т. е. янтарная и глутаровая кислоты, при нагревании отщепляют элементы воды и дают внутренние циклические ангидриды:

3. Непредельные карбоновые кислоты
Состав непредельных одноосновных кислот с одной двойной связью можно выразить общей формулой С n Н 2 n -1 СООН. Как и для любых бифункциональных соединений, для них характерны реакции как кислот, так и олефинов. α.β-Непредельные кислоты несколько превосходят по силе соответствующие жирные кислоты, так как двойная связь, находящаяся рядом с карбоксильной группой, усиливает ее кислотные свойства.
Акриловая кислота. Простейшая непредельная одноосновная кислота
Олеиновая, линолевая и линоленовая кислоты.
Олеиновая кислота С 17 Н 33 СООН в виде глицеринового эфира чрезвычайно распространена в природе. Ее строение выражается формулой
Олеиновая кислота - бесцветная маслянистая жидкость, легче воды, на холоду затвердевает в игольчатые кристаллы, плавящиеся при 14 °С. На воздухе она быстро окисляется и желтеет.
Молекула
олеиновой кислоты способна присоединять
два атома галогена:
В присутствии катализаторов, например Ni, олеиновая кислота присоединяет два атома водорода, переходя в стеариновую кислоту.
Олеиновая кислота представляет собой цис-изомер (все природные непредельные высокомолекулярные кислоты, как правило, относятся к цис-ряду).
Линолевая С 17 Н 31 СООН и линоленовая С 17 Н 29 СООН кислоты еще более ненасыщены, чем олеиновая кислота. В виде сложных эфиров с глицерином - глицеридов - они являются главной составной частью льняного и конопляного масел:

В молекуле линолевой кислоты две двойные связи. Она может присоединять четыре атома водорода или галогена. В молекуле линолевой кислоты три двойные связи, поэтому она присоединяет шесть атомов водорода или галогена. Обе кислоты, присоединяя водород, переходят в стеариновую кислоту.
Сорбиновая кислота
Она имеет две сопряженные друг с другом и с карбоксильной группой двойные связи, имеющие транс-конфигурацию; является прекрасным консервантом для многих пищевых продуктов: овощных консервов, сыра, маргарина, фруктов, рыбных и мясных продуктов.
Малеиновая и фумаровая кислоты. Простейшими из двухосновных кислот, содержащих этиленовую связь, являются два структурных изомера:

Кроме того, для второй из этих кислот возможны две пространственные конфигурации:

Фумаровая кислота содержится во многих растениях: особенно часто она встречается в грибах. Малеиновая кислота в природе не найдена.
Обе кислоты обычно получают при нагревании яблочной (оксиянтарной) кислоты:
При медленном, осторожном нагревании получается главным образом фумаровая кислота; при более сильном нагревании и при перегонке яблочной кислоты получается малеиновая кислота.
Как фумаровая, так и малеиновая кислота при восстановлении дают одну и ту же янтарную кислоту.
Все началось с уксуса, по крайней мере, открытие карбоновых кислот . Название объединяет органические соединения, содержащие карбоксильную группу COOH.
Важно расположение атомов именно в таком порядке, поскольку есть и другие кислородосодержащие соединения.
Уксусную из карбоновых открыли первой, но ее строение многие века оставалось тайной. Вещество знали, как продукт скисания вин.
Как соединение 2-ух атомов , 4-ех и 2-ух кислорода стала известна миру лишь в 18-ом столетии.
После, открыли целый ряд карбоновых . Ознакомимся с их классификацией, общими свойствами и областями применения.
Свойства карбоновых кислот
Отличаясь от другой органики наличием карбоксильных групп, карбоновые кислоты классифицируются по их числу.
Есть одно-, двух-, и многоосновные соединения. Одноосновные карбоновые кислоты выделяются связью между карбоксильной группой и углеводородным радикалом.
Соответственно, общая формула веществ группы: — C n H 2 n +1 COOH. Уксусная – одноосновная. Ее химическая запись: — CH 3 COOH. Еще проще строение соединения: — COCOOH.
К простейшим отнесена и с формулой C 2 H 5 COOH. У остальных соединений одноосновного ряда есть изомеры, то есть, разные варианты строения.
У муравьиной же, уксусной и пропионовой есть лишь один план строения.
Если у карбоновой кислоты формула с двумя карбоксильными группами, она может называться диосновной.
Общая запись веществ категории: — COOH-R-COOH. Как видно, карбоксильные группы располагаются по разные стороны линейной молекулы.
В многоосновных карбоксильных радикалов, как минимум три. Два стоят по краям молекулы, а остальные крепятся к центральным атомам углерода. Такова, к примеру, лимонная . Пространственная запись ее формулы: —

Подразделяют карбоновые соединения и по характеру углеводородного радикала. Химические связи между его атомами могут быть одинарными.
В этом случае перед нами предельные карбоновые кислоты. Наличие двойных связей указывает на непредельные вещества.
Формула непредельных карбоновых кислот может одновременно являться записью высших представителей класса.
Высшими называют соединения, в которых боле 6-ти атомов углерода. Соответственно, от 1-го до 5-ти атомов углерода – признак низших веществ.
Высшие карбоновые кислоты – это, к примеру, , , линоленовая, пальмитиновая и арихидоновая. В полследней 21 атом углерода, в остальных по 18.
Имея органическое происхождение, большинство карбоновых пахнут, хотя бы слегка. Однако, есть группа особенно ароматных.
В их состав входит бензольное ядро. То есть, группы являются производными бензола. Его формула: — C 6 H 6 .
У вещества сладковатый запах. Поэтому, карбоновые с бензольным ядром именуют ароматическими. Причем, обязательна прямая связь ядра и карбоксильных групп.
По физическому состоянию карбоновые бывают, как жидкими, так кристаллическими. Имеется в виду агрегатность веществ при обычных условиях.
Часть соединений растворима в воде, другая часть смешивается лишь с органикой. Нюансы химического поведения зависят от количества в молекулах карбоксильных групп.
Так, типичная реакция карбоновых кислот одноосновной категории– окрашивание лакмусовой в цвет.
Классикой, так же, считается взаимодействие с галогенами, тогда как дикарбоновые соединения могут образовывать эфиры карбоновых кислот. Они «рождаются» во взаимодействии со спиртами.
Карбоновая кислота с двумя основаниями всегда содержит метиленовую группу, то есть, двухвалентную CH 2 .
Ее наличие между карбоксильными группами повышает кислотность атомов водорода. Поэтому, возможна конденсация производных . Это еще одно объяснение появления эфиров.
Двухосновные соединения образуют, так же, соли карбоновых кислот . Они используются на производстве моющих средств, в частности, мыла.
Впрочем, о том, где пригождаются карбоновые кислоты и их соединения, поговорим отдельно.
Применение карбоновых кислот
В производстве мыла особенно важны стеариновая и пальмитиновая кислоты. То есть, используются высшие соединения.
Они делают мыльные брикеты твердыми и позволяют смешать фракции, расслаивающие без присутствия кислот.
Способность делать массы однородными пригождается и на производстве лекарств. Большинство связующих элементов в них – карбоновые кислоты.

Соответственно, применение реагентов внутрь, как и наружно, безопасно. Главное, знать предельную дозировку.
Превышение дозы, или концентрации кислот, ведет к разрушительным последствиям. Возможны химические ожоги, отравления.
Зато, едкость соединений наруку металлургам, мебельщикам, рестовраторам. Им карбоновые кислоты и смеси с ними помогают полировать и очищать неровные, заржавевшие поверхности.
Растворяя верхний слой металла, реагенты улучшают его внешний вид и эксплуатационные характеристики.
Химические карбоновые кислоты могут быть очищенными, или же, техническими. Для работы с металлами подойдут и последние.
Но, в качестве косметических и лекарственных средств применяют лишь высокоочищенные соединения. Такие нужны и в пищевой промышленности.
Около трети карбоновых кислот – официально зарегистрированные добавки, известные простым обывателям, как ешки.
На упаковках они отмечаются букврй Е и порядковым номером рядом с ней. Уксусная кислота, к примеру, пишется, как Е260.
Пищей карбоновые кислоты могут служить и для растений, входя в состав удобрений. Одновременно, можно создавать яды для вредоносных насекомых и сорняков.
Идея заимствована из природы. Ряд растений самостоятельно вырабатывают карбоновые кислоты, дабы близ них не было других трав, конкурирующих за почву и ее ресурсы. При этом, вырабатывающие яд растения, сами имеют к нему иммунитет.
Около трети карбоновых соединений используют в качестве протрав для тканей. Обработка необходима, чтобы материи равномерно окрашивались. С этой же целью реактивы применяют в кожевенной промышленности.
Добыча карбоновых кислот
Поскольку карбоновые кислоты биогенны, около 35% из них получают из природных продуктов. Но, химический синтез выгоднее.
Поэтому, при возможности переходят на него. Так, гиалуроновую кислоту, используемую для омоложения, долгое время добывали из пуповин младенцев и крупного рогатого скота.
Теперь же, соединение получают биохимическим способом, выращивая на пшеничном субстрате бактерий, беспрерывно дающих кислоту.
Получение карбоновых кислот чисто химическим путем – это окисление спиртов и альдегидов.
Под последним понятием скрываются спирты, лишенные водорода. Реакция протекает так: — СН 3 – СН 2 ОН → СН 3 – СОН → СН 3 – СООН.
Ряд карбоновых кислот получают гидролизом сложных эфиров. Получая в свой состав воду, они преобразуются в героинь .

Сформировать их можно и из моногалогенпроизводных. Кислоты из них получаются под действием цианида . Полупродукт реакции необходимо разложить водой.
От схемы производства, количества его ступеней, расходных материалов, во многом зависит стоимость конечных продуктов. Узнаем, каков ценник на карбоновые кислоты в их чистом виде.
Цена карбоновых кислот
Большинство карбоновых кислот продают большими объемами. Фасуют, обычно, по 25-35 килограммов. Жидкости разливают в канистры.
Порошки засыпают в полиэтиленовые пакеты, а стеариновую кислоту, вообще, заворачивают в . Ценник, обычно, выставляется за кило.
Так, 1000 граммов лимонной кислоты стоит в районе 80-ти рублей. Столько же берут за муравьиную и щавелевую.
Стоимость олеиновой – около 130-ти рублей за килограмм. Салициловая кислота оценивается уже в 300. Стеариновая кислота на 50-70 рублей дешевле.
Ряд карбоновых кислот оценивается в долларах, поскольку основные поставки ведутся из США и стран Евросоюза.
Оттуда поступает, к примеру, гиалуроновая кислота. За килограмм отдают уже не пару сотен рублей, а несколько сот баксов.

Отечественный продукт присутствует, но ему не доверяют, в первую очередь, клиенты красоты.
Они знают, что омоложение с помощью гиалуроновой кислоты – придумка американцев, практикуемая ими полвека.
Соответственно, велика практика производства препарата, который должен быть качественным, ведь попадает в кожу и организм.
Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 .
2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
| ЗNаОН | ||||
| R-CCl 3 | → | R — COOH + Н 2 О | ||
| -3NaCl |
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/>
СН 3 -В r + NaCN → CH 3 — CN + NaBr .
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH 3 CN + 2Н 2 О → CH 3 COONH 4 .
При подкислении раствора выделяется кислота:
CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl .
4 . Использование реактива Гриньяра по схеме:/>
Н 2 О
R
—
MgBr
+ СО 2 →
R
—
COO
—
MgBr
→
R
—
COOH
+
Mg
(OH
)
Br
5 . Гидролиз сложных эфиров:/>
R — COOR 1 + КОН → R — COOK + R ‘ OH ,
R — COOK + HCl → R — COOH + KCl .
6 . Гидролиз ангидридов кислот:/>
(RCO ) 2 O + Н 2 О → 2 RCOOH .
7 . Для отдельных кислот существуют специфические способы получения./>
Муравьиную кислоту получают нагреванием оксида углерода ( II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О.
Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия:
5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O .
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта):
Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/>
RCOOH
![]() RCOO — + Н +
RCOO — + Н +
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . />
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
|
Карбоновые кислоты Формула K a |
|
Пропионовая CH 3 CH 2 COOH 1,3*10 -5 |
|
Масляная CH 3 CH 2 CH 2 COOH 1,5*10 -5 |
|
Уксусная CH 3 COOH 1,7*10 -5 |
|
Кротоновая CH 3 — CH = CH — COOH 2,0*10 -5 |
|
Винилуксусная CH 2 =CH-CH 2 COOH 3,8*10 -5 |
|
Акриловая CH 2 =CH-COOH 5,6*10 -5 |
|
Муравьиная HCOOH 6,1*10 -4 |
|
Бензойная C 6 H 5 COOH 1,4*10 -4 |
|
Хлоруксусная CH 2 ClCOOH 2,2*10 -3 |
|
Тетроновая CH 3 — C ≡ C — COOH 1,3*10 -3 |
|
Дихлоруксусная CHCl 2 COOH 5,6*10 -2 |
|
Щавелевая HOOC — COOH 5,9*10 -2 |
|
Трихлоруксусная CCl 3 COOH 2,2*10 -1 |
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 ,
2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О,
RCOOH + NaOH → RCOONa + Н 2 О,
RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 .
Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей:
CH 3 COONa + HCl → СН 3 СООН + NaCl .
Соли карбоновых кислот в водных растворах гидролизованы:
СН 3 СООК + Н 2 О
![]() СН 3 СООН + КОН.
СН 3 СООН + КОН.
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных.
3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу ( R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот.
Хлорангидриды получают действием хлорида фосфора ( V ) на кислоты:
R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
|
Соединение примеры |
|
Кислота
Этановая(уксусная) Бензойная кислота хлорангидрит кислоты
Этаноилхлорид Бензоилхлорид (ацетилхлорид) ангидрид кислоты
Этановый(уксусный) бензойный ангидрит Ангидрит сложый эфир
Этилэтаноат(этилацетат) Метилбензоат амид Этанамид(ацетамид) Бензамид Нитрил Этаннитрил Бензонитрил (ацетонитрил) |
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств:
2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 .
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
Механизм реакции этерификации был установлен методом "меченых атомов".
Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl .
Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов :
СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl .
Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот:
При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
| Р 2 0 5 | ||
| CH 3 — CO — NH 2 |
→ |
CH 3 — C ≡ N + Н 2 О |
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты:
R-CO-X + Н 2 О →R-CO-OH + НХ .
В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например:
R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH.
4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
| р кр | ||
|
СН 3 -СН 2 -СООН + Вr 2 |
→ |
СН 3 -СНВr-СООН + НВr |
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН,
СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН,
СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН,
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН,
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .

5 . Окислительно-восстановительные реакции карбоновых кислот./>
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды:
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:
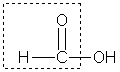
Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" :
НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
или в упрощенном виде:
C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О.
Кроме того, муравьиная кислота окисляется хлором:
НСООН + Сl 2 → СО 2 + 2 HCl .
В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О:
СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О.
6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/>
Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования :
Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании: